His story
[K.SJ, 일상 이야기] 코로나19(COVID-19) - (13) 2020년 3월, 국산 코로나19 진단키트 FDA (긴급사용) 승인은 왜 비공개일까? 4월 미국 긴급 수출 세 곳 업체, EUA 승인 업체 현황 업데이트 본문
[K.SJ, 일상 이야기] 코로나19(COVID-19) - (13) 2020년 3월, 국산 코로나19 진단키트 FDA (긴급사용) 승인은 왜 비공개일까? 4월 미국 긴급 수출 세 곳 업체, EUA 승인 업체 현황 업데이트
K.SJ 2020. 3. 30. 00:09# 신종 코로나 바이러스 감염증 (코로나 19, COVID-19)은 시간이 걸리더라도 반드시 극복 할 겁니다.
그 때, 지금의 일들을 잊지 않기 위해서 기억하기 위해 글을 남깁니다.
[K.SJ, 일상 이야기] 신종 코로나바이러스 감염증 (코로나19, COVID-19) - (13) 2020년 3월, 국산 코로나19 진단키트 FDA (긴급사용) 승인은 왜 비공개일까? 4월 미국 긴급 수출한 세 업체, EUA 승인 받은 업체 현황 업데이트
우리나라에서 코로나 19의 확산세가 줄어들 수 있었던 요인 중 하나로, 광범위한 코로나 19의 검진을 외국에서도 많이 들고 있습니다.
미국의 확산세가 지속되자 트럼프 대통령이 문재인 대통령에게 의료장비 지원을 요청했고, 문재인대통령도 FDA 승인 등에 대한 요청을 한바 있습니다.
진단 키트 관련,
3월 28일(토) 외교부에서 “코로나 19 국산 진단키트 3개 제품이 미 FDA 긴급 사용 승인 절차상 사전 승인 획득” 이라고 발표 했습니다.
* (참고) EUA는 Emergency Use Authorization(긴급 사용 승인)의 줄임말입니다.
1. 대한민국 외교부 홈페이지에 들어가서 검색해보니, 관련 내용은 없었습니다.
2. 미국 FDA 홈페이지 확인
- FDA 사이트에도 들어가서 확인해보니, 3월 27일까지 내용이 업데이트 되어 있는데, 국산 진단 키트 업체 관련 내용은 없었습니다.
(업데이트 되지 않은 걸까요?)
- 4월 18일자 업데이트 내용이 있습니다. 아래 6번을 확인하세요!
- 4월 29일자 업데이트 내용이 있습니다. 아래 7번을 확인하세요!
Emergency Use Authorization
Emergency Use Authorization (EUA) information, and list of all current EUAs
www.fda.gov
3. (기사검색) 혹시나 싶어 나스닥닷컴이라는 사이트에 들어가봤습니다.
(클릭) https://www.nasdaq.com/articles/covid-19-diagnostic-tests-2020-03-20


위의 링크를 클릭해서 들어가보면,
한국 업체 중 씨젠의 경우만 표기 되어 있는데 이마저도 “CE mark” 와 한국 식약처 관련 표기만 되어 있었습니다.

4. 씨젠, EDGC 관계자 등 국산 진단키트 업계 관련자들의 의견을 포함한 기사가 떴습니다.
(클릭) https://news.naver.com/main/read.nhn?mode=LPOD&mid=sec&oid=001&aid=0011506539&isYeonhapFlash=Y&rc=N
국산 진단키트 3개 미국 FDA 사전승인?…"외교부가 혼란 초래"
FDA 긴급사용승인 목록에 국내업체 없어…"미국서 국산 키트 이미 사용 중" (서울=연합뉴스) 김잔디 기자 = 국산 신종 코로나바이러스 감염증(코로나19) 진단키트 3개가 미국 식품의약국(FDA)의 '사전 승인'을
news.naver.com
이미 수출을 하고 있는 업체에서도 해당 내용은 들은 바가 없다고 하는데 과연 누구의 말이 맞을지 궁금합니다. 그리고, 29일(토) 외교부에서 왜 굳이 3개 업체라고 꼽아서 이야기를 하되, 해당 업체명은 이야기 하지 않았는지도 궁금합니다. 주말을 끼어서 발표를 했어야만 했을까요? 그리고 3개 업체 이후에 추가 사전 승인을 득할 수 도 있는데, 관련 내용은 언급되지 않은 것도 의문입니다.
업체명은 밝히지 않아 많은 사람들이 3개의 업체가 어디인지 궁금해 하는 상황입니다. (저 역시 궁금합니다.)
월요일에 어떤 내용들이 업데이트 될지 지켜봐야겠습니다.
+
4월 1일(수)까지도 3개 업체가 어디인지 공개되지 않았습니다. 다들 궁금해 하는데...
FDA 사이트에서도 여전히 미공개 중이고, 과연 해당 업체는 어디일까요???
+ (업데이트) 2020년 4월 미국 긴급 수출한 세 업체?!
5. 코로나19 진단 키트 수출 업체 관련 기사 : 기사를 보면 1차로 솔젠트(SolGent) 15만 테스트 분량을 미국으로 발송했고, 2차로 60만 테스트 분량은 4월 15일에 도착예정이라고 했습니다. (2차 공급 업체는 오상 헬스케어와 SD 바이오센서라고 합니다.)
1) 미국 NBC 계열 지역 방송국인 NBC Palm springs 기사입니다. (이 방송도 CNN 방송을 인용했습니다.)
(클릭) https://www.google.com/amp/s/nbcpalmsprings.com/2020/04/13/us-to-receive-750000-coronavirus-tests-from-south-korea/amp/
US to Receive 750,000 Coronavirus Tests from South Korea
The United States is turning to South Korea — a country with an aggressive testing regime that President Donald Trump previously downplayed — to bring approximately 750,000 more coronav…
nbcpalmsprings.com

한국에서도 연합뉴스에서 기사가 나왔습니다.
[참고기사] SD바이오센서·솔젠트·오상헬스, 코로나19 진단키트 미국수출(2020년 4월 14일자, 연합뉴스, 김잔디 기자님)
(클릭) https://news.naver.com/main/read.nhn?mode=LSD&mid=sec&oid=001&aid=0011548246&sid1=001
SD바이오센서·솔젠트·오상헬스, 코로나19 진단키트 미국수출<CNN>
코로나19 진단키트 75만회 검사분량·1천140만 달러 규모 (서울=연합뉴스) 김잔디 기자 = SD바이오센서와 솔젠트, 오상헬스케어, 등 국내 3개 진단전문기업이 미국에 75만회 검사 분량의 신종 코로나바이러스 감염
news.naver.com
외교부에서 업체 공개를 꺼리는 부분은
아무래도 업체 공개에 따른 주식 가격 변동의 여파가 있을 수 있어 공개를 하지 않고 있다는 생각도 들었습니다.
6. (업데이트) 2020년 4월 18일자 오상헬스케어, 미 FDA 긴급 사용 승인받음
사이트에 들어가서 COVID-19 EUA리스트를 보면
맨 아래에 오상 헬스케어 이름을 확인 할 수 있습니다. 4월 18일자로 긴급승인을 받았습니다.
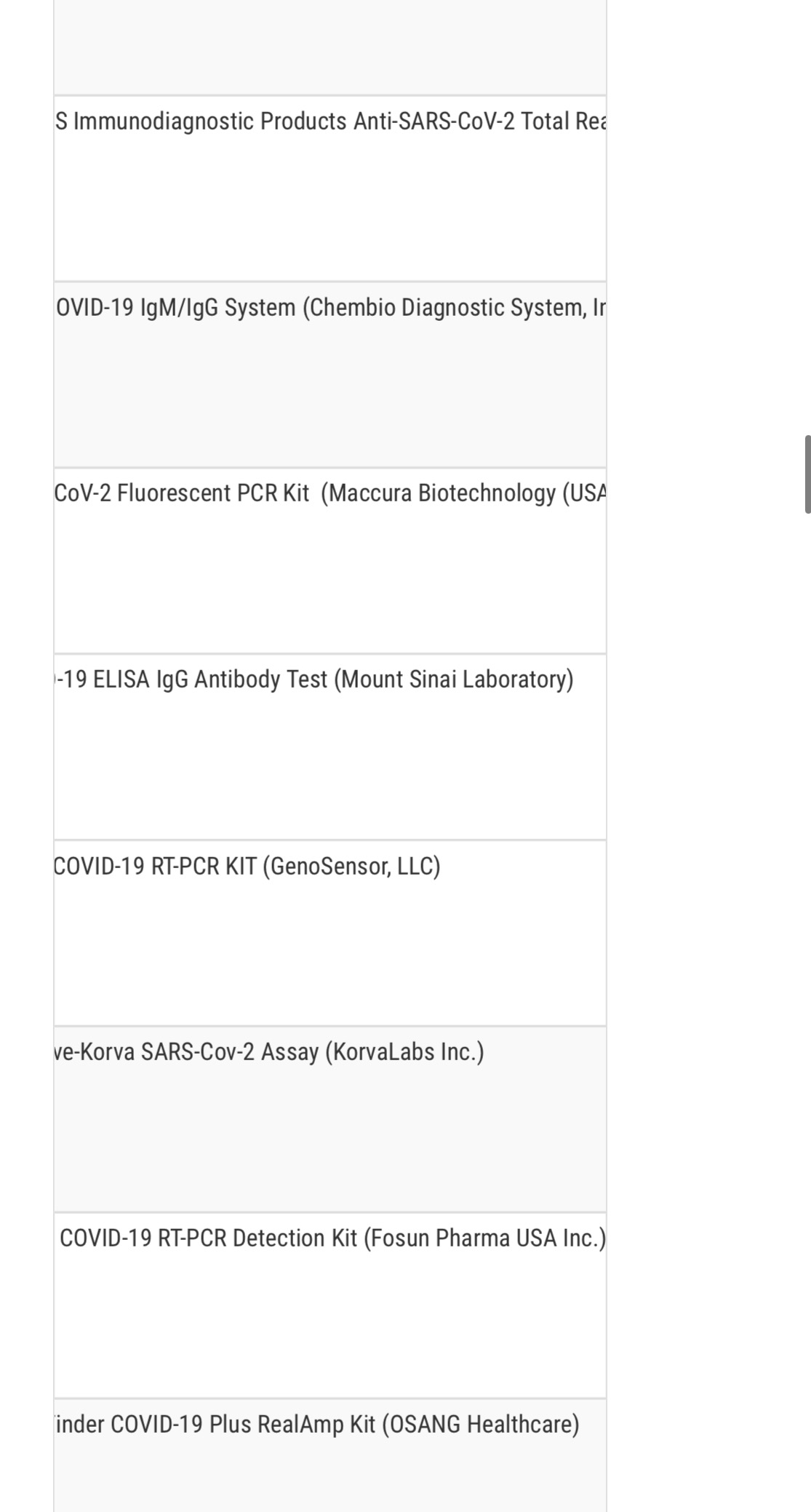

오상 헬스케어가 미 FDA EUA를 받았다면, 나머지 다른 두 곳은 어디일까요?
궁금해집니다.
7. (업데이트) 추가 미 FDA 긴급 승인(EUA) 업체
4월 21일자 씨젠, 미 FDA 긴급 사용(EUA) 승인받음.
4월 23일자, SD 바이오센서 미 FDA 긴급 사용(EUA) 승인받음.
4월 29일자, 랩지노믹스 긴급 사용(EUA) 승인받음
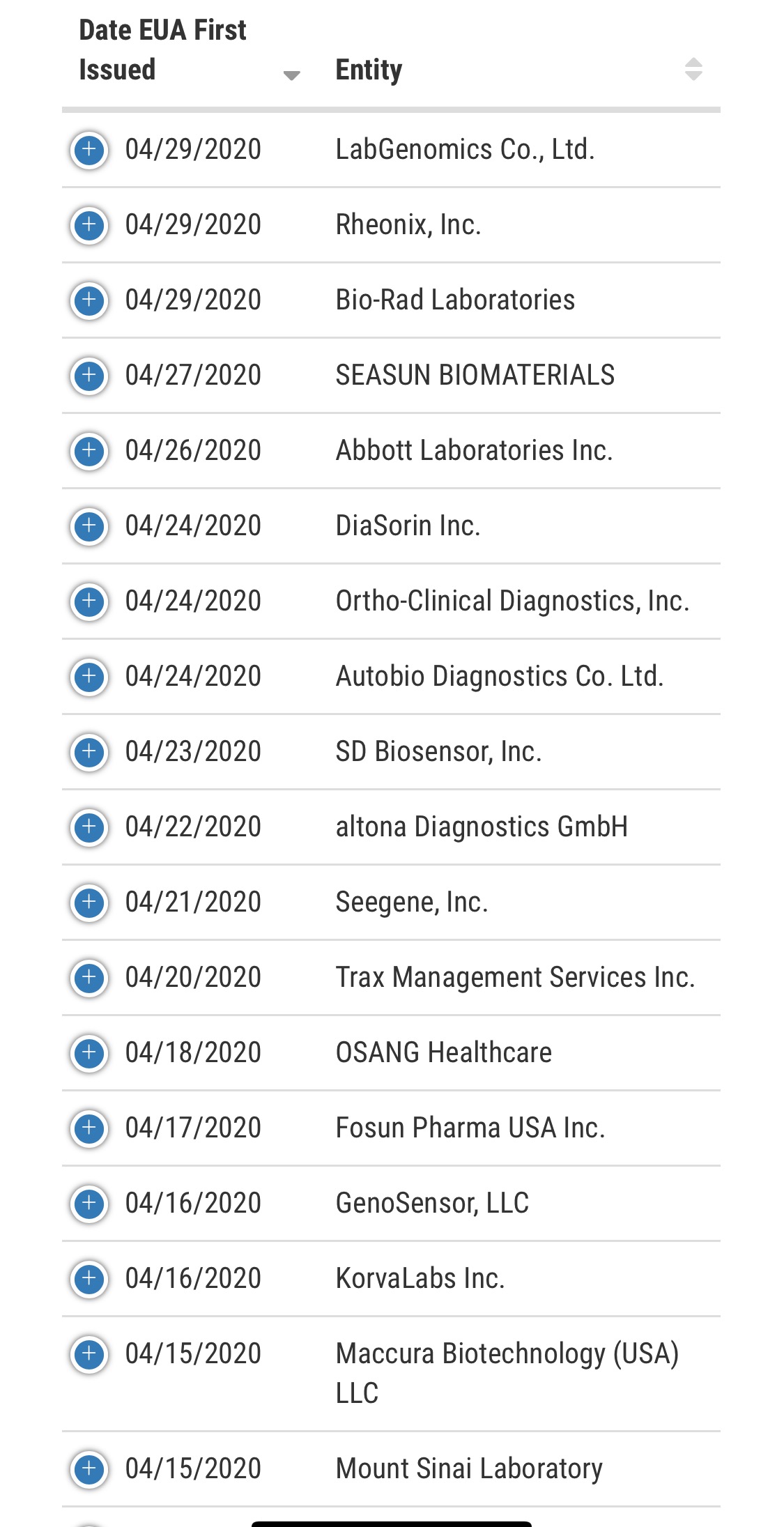
정리를 해보면
4월 18일자, 오상헬스케어, 미 FDA 긴급 사용(EUA) 승인받음
4월 20일자, 휴마시스, 코로나19 항체 진단키트 미 FDA 제품 등록
4월 21일자, 씨젠, 미 FDA 긴급 사용(EUA) 승인받음.
4월 23일자, SD 바이오센서 미 FDA 긴급 사용(EUA) 승인받음.
4월 29일자, 랩지노믹스 긴급 사용(EUA) 승인받음.
추가적으로 미 FDA 긴급 사용 승인 받는 업체는 어디일까요?
그리고, 항체 검사뿐 아니라 백신 등 치료약 개발도 주요 화두가 되고 있는데, 어느 나라, 어느 업체가 먼저 개발을 할지도 궁금해집니다.
[휴마시스 관련 참고기사]
韓 코로나 진단키트 잇단 美 긴급승인…세계가 주목(2020년 4월 26일자, 뉴시스, 송연주 기자님)
(클릭) https://newsis.com/view/?id=NISX20200424_0001005638&cID=13001&pID=13000
韓 코로나 진단키트 잇단 美 긴급승인…세계가 주목
[서울=뉴시스] 송연주 기자 = 한국의 코로나19 진단키트가 미국 식품의약국(FDA)의 높은 장벽을 넘어 잇달아 시판 승인을 받고 있다
www.newsis.com
(도움이 되셨다면 아래의 공감(하트표시) 한번 꾸욱~ 눌러주세요, 큰 격려가 됩니다. ^^)
* 공감은 별도 로그인 없이도 가능합니다.
* 공감은 페이스 북의 "좋아요"의 의미로 보시면 됩니다. 좋은 정보는 공유하고 싶은 마음에... 부탁 드립니다. ^-^
* 네이버, 구글에서 K.SJ, Review 로 검색하시면 더 많은 글을 보실 수 있습니다.
* 수정이 필요한 사항은 댓글이나, 방명록에 남겨주시면 수정하겠습니다